水の電気分解まるわかり! 化学反応式のつくりかた、わかりやすく解説
化学変化(化学反応)とは、「もとの物質」とは違う、「別の物質」ができる変化です。
化学反応式は、「化学変化を化学式で表したもの」です。「もとの物質」と、化学変化によってできた「別の物質」を矢印(→)で結んだものです。

水の電気分解を例に、化学反応式を作ってみましょう。
水の分解では、「水」が分かれて、「水素」と「酸素」になります。反応前の物質は、水です。反応後の物質は、水素と酸素です。反応前の物質と反応後の物質を矢印でつなぐと、こうなります。
水→水素+酸素
次に、物質名を化学式に置き換えてみます。
H2O→H2+O2
でも、上の式は、まだ完成ではありません。というのも、化学反応式では矢印の左側と右側で原子の種類と数が同じであるからです。
矢印の左側と右側で、原子の数を数えてみましょう。
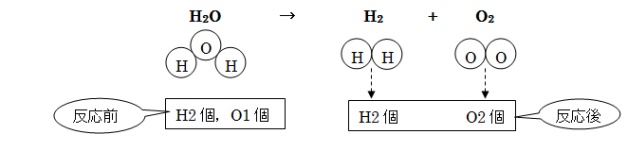
左側ではHが2つ、Oが1つ。右側ではHが2つ、Oが2つあります。数がそろっていませんね。
左側のH2Oを、Oが2つになるようにするためには、H2Oを2個にします。
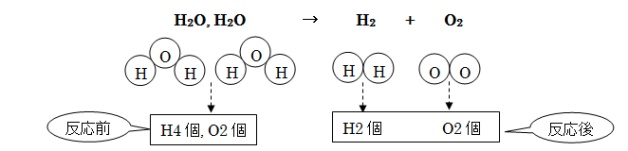
矢印の左側と右側で、Oの数がそろいました。今度はHの数を比べてみます。左側にHが4つあるので、右側のH2を2個にすれば、すべての原子の数がそろいます。
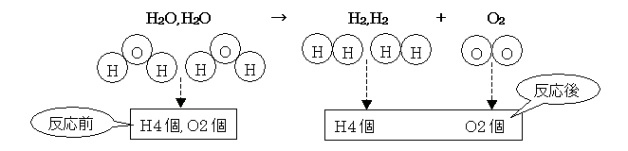
最後に、物質(化学式)ごとにまとめます。
矢印の左側では、H2Oが2個なので、2を化学式H2Oの前につけ、「2H2O」と表します。同じように、矢印の右側ではH2が2個なので「2H2」、O2は1個なのでそのまま「O2」と表します。
2H2O→2H2+O2
これで完成です!
↓くわしくは、こちらのサイトで!『教科質問ひろば』
みなさんがよく疑問に思うことを、教科ごとにわかりやすく解説していますよ。
つまずきがちな単元も、しっかり解決してくれるはずです!!