【反応熱】なぜ物質の状態を書くのか?
熱化学方程式を作るときに,なぜ必ず化学式の後にその物質の状態,すなわちその物質が気体であるのか,液体なのかそれとも固体なのかを書く必要があるのですか?
進研ゼミからの回答
こんにちは。いただいた質問について回答します。
【質問内容】
【問題】
水素の燃焼熱は286kJ/molである。このときの反応熱をもとに熱化学方程式を書け。ただし,生成する水は
液体であるとする
という問題について,解答として

【質問への回答】
熱化学方程式は,熱エネルギーに関する等式です。左辺の物質のもつエネルギーの総和と,右辺の物質の
もつエネルギーと反応熱の総和が等しいという意味を表しています。
例えば,次の熱化学方程式を見てください。

次に,水を例に見てみましょう。
皆さんがよく知っている通り,我々の身の回りに存在している大変なじみの深い水は,あるときには氷(固体)
として存在し,あるときには水道から出てくる液体の水,そしてまたあるときには水蒸気(気体)として存在する
ことがあります。
氷を加熱すると液体の水になり,さらに液体の水を加熱すると水蒸気になりますね。加熱するということはエ
ネルギーを与えるということですから,氷より液体の水,液体の水より水蒸気のほうがエネルギーが大きいこ
とがわかります。具体的には次のようになっています。
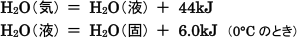
つまり,水の場合,これだけ固体のときと液体のとき,気体のときではエネルギーに差があるわけです。です
から,上の(1)式において,水の状態が書かれていないと,気体の場合なのか液体なのか,あるいは固体な
かわからなくなり,熱化学方程式が成立しなくなるわけです。
その物質の状態がわかりきっている場合(例えば水素や酸素は普通は気体であるなどという場合)には,
化学式の後に(気),(液),(固)と書くのを省略して構いません。したがって,「水素の燃焼熱は286kJである
(生成した水は液体)」ことを表す熱化学方程式を
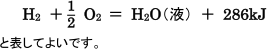
【学習アドバイス】
熱化学方程式を立てるとき,物質の状態を書くべきか迷うことがあります。
・ 水やアルコールなど蒸発しやすい物質
・炭素(黒鉛,ダイヤモンド)など同素体をもつ単体
については,常温における状態が複数ありうるので,物質の状態を書いておくようにしましょう。そのほかの
状態が明らかな物質については,状態を書かなくて構いませんが,慣れないうちは,熱化学方程式中の化
学式の後には必ず物質の状態を書いておくとよいでしょう。
今後も『進研ゼミ高校講座』を使って,得点を伸ばしていってくださいね。