【気体の性質】混合気体の反応後の量を求める過程がわかりません。
混合気体の反応の問題で,反応後の量を求めるときに出てくる表のようなものが,どのようにして出てくるのかがわかりません。作るコツなどはあるのですか?
進研ゼミからの回答
こんにちは。いただいた質問について回答します。
【質問内容】

【質問への回答】
この表は,最初からすべての数値が入っているわけではなく,化学反応の量的関係をもとに,わかっている
数値を順に入れて出来上がったものです。次の手順で求めていきます。
①化学反応式を書く
まずは量的関係を追跡していくためにも,化学反応式を書き出します。結果だけ書き出すと次の通りです。
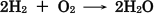
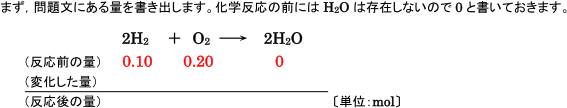
②反応前の量,変化した量,反応後の量を物質量で書き出す
(化学反応式の係数の比)=(反応した物質量の比)なので,化学反応式の下にわかっている量を書き出し,
物質量の変化を追跡していきます。このとき,値がわからないところはいったん空欄のままにしておき,ス
ペースをあけておくことがコツです。
次に,反応終了後の量を考えます。水素も酸素も容器の中の量は有限なので,反応物の一方(どちらか一
つでも)がなくなると,ほかの反応物が残っていても反応は終了してしまいます。問題文にはなくなった物質
がどちらであるか書いていないので,まず水素が完全に反応したと考えて計算を進めます。このとき,反応
後の水素の量は0molとなります。

続いて,(化学反応式の係数の比)=(反応した物質量の比)から,水素以外の物質量の変化を考えます。
反応した物質量の比は

【学習アドバイス】
混合気体における反応の量的関係の問題では,どちらかが完全になくなるまで反応が進んだ後の物質量を
考える問題がよく出題されます。化学反応式について学習したときと同様に,
①化学反応式を書き出し,
②反応前の量,変化した量,反応後の量を物質量で書き出す
ことにより,何がどれだけ反応したのかを順を追って考えるようにしましょう。その際,一気に答えは出ないこ
とが多いので,わからない量を明確にしたうえで,上記で説明したような手順で一つひとつわかった量を書き
出していくようにしましょう。
また,反応物の量が物質量ではなく体積[L](または[mL])や質量[g]などで表されていることが多いので,
表に書き出す前に
●与えられた物質の量を物質量[mol]に変換しておく
ことを忘れないようにしましょう。
今後も『進研ゼミ高校講座』を使って,得点を伸ばしていってくださいね。